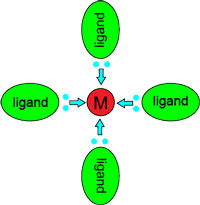
 Een complex is een verbinding waarbij een metaalion wordt omringd door liganden. Een ligand is een molecuul of ion met één of meer vrije elektronenparen. Het ligand geeft als het ware zijn elektronenpaar aan het centraalatoom. Te leen. Want de elektronen gaan niet helemaal naar het centraal atoom. Je kan ook zeggen: "niet voortdurend".
Een complex is een verbinding waarbij een metaalion wordt omringd door liganden. Een ligand is een molecuul of ion met één of meer vrije elektronenparen. Het ligand geeft als het ware zijn elektronenpaar aan het centraalatoom. Te leen. Want de elektronen gaan niet helemaal naar het centraal atoom. Je kan ook zeggen: "niet voortdurend".
Als het complex uit elkaar valt gaan de elektronen gewoon weer mee met het ligand.
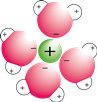
Water is zo'n ligand. De negatieve kant van het watermolecuul hecht zich aan een positief ion.
Een gehydrateerd metaalion is dus een complex.
EDTA
Een bijzonder ligand is edta (ethyleendiaminetetraazijnzuur). Het EDTA-molecuul heeft 6 elektronegatieve groepen met daarin vrije elektronenparen:
* 4 carboxylgroepen (rood) * 2 aminogroepen (blauw)
Onder: in de zwarte cirkels zie je de 6 elektronegatieve groepen. Het molecuul vouwt zich rond een metaalion: rechts in het plaatje.
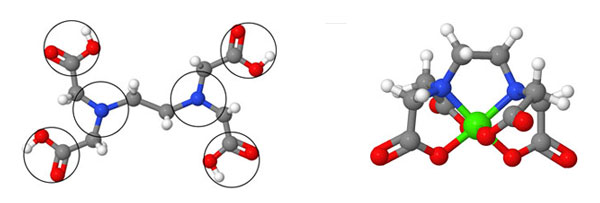 EDTA is daardoor een 6-tandig ligand. Een metaalion wordt door het molecuul "gevangen in een kooi" als het ware.
EDTA is daardoor een 6-tandig ligand. Een metaalion wordt door het molecuul "gevangen in een kooi" als het ware.
Met EDTA kun je heel goed metaalionen titreren. Dit noemen we complexometrie.
Eigenschappen complexometrie:
* EDTA in de buret
* pH in het titratievat hangt af van het te "vangen" ion, in de regel: licht basisch of neutraal.
* de indicator geeft zelf een gekleurd complex met het metaalion, om alle ionen met EDTA te vangen moet je dus door titreren tot de kleuromslag volledig is.
Terminologie
Vooral in het Engels kom je verschillende benamingen tegen voor complexen:
| complex | complex |
| coördination compound | complex |
| chelate (spreekuit: kieleete) | complexvormer, dus eigenlijk meer het ligand |
| masking agent | maskeer-middel, complexvormer, dus eigenlijk het ligand |
Hard water
Hard water bevat veel calcium en mogelijk magnesium-ionen. Maar het gaat vooral om Ca2+. De belangrijkste nadelen van hard water:
* Ca2+ reageert met anionogene zeepmoleculen, dus zeep dat een negatief ion is. Er is dan meer zeep nodig voor het wasproces.
Het calcium-zeep neerslag draagt bij aan de "grauwsluier". Bij het handenwassen met hard water merk je het ook.
* Ca2+ reageert met carbonaat dat uit HCO3- ontstaat bij verwarmen: 2 HCO3- ---> H2O + CO32- Ca2+ + CO32- ---> CaCO3↓
Dit calciumcarbonaat is het bekende "ketelsteen". De afzetting op verwarmingselementen in de wasmachine of in het koffiezetapparaat.
Hardheid is belangrijk in het dagelijks leven maar ook in fabrieken waar water gebruikt wordt. Daarom wordt de hardheid veel gemeten. De hardheid verschilt in Nederland per regio:
verder....
