Chemisch rekenen: blijf oefenen!
Onderstaand voor enkele typen berekeningen nog eens enkele handvatten en of adviezen....
Oplossen en verdunnen
Bedenk altijd dat bij het maken van een verdunning ....
- het volume groter wordt,
- de hoeveelheid opgeloste stof gelijk blijft,
- de verdunningsfactor het grote volume gedeeld door het kleine volume is.
Titreren
Bij het titreren zijn er in hoofdzaak twee typen berekeningen: gehaltebepaling en titerstelling. Een berekening van een gehaltebepaling verloopt altijd volgens onderstaand schema.
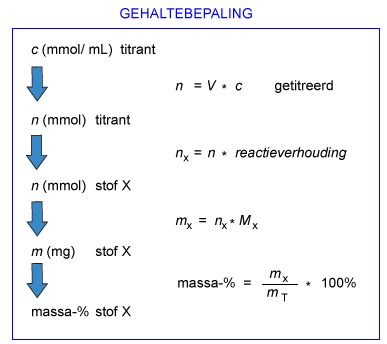
Een titratieberekening waarbij je de sterkte titrant (titer) berekent, verloopt altijd als volgt:

Avogadro
Gassen zijn stoffen waarvan de moleculen (of atomen bij edelgassen) vrij bewegen. Een gas waarvan de moleculen elkaar helemaal niet aantrekken of afstoten noemen we een ideaal gas. Echte gassen zijn niet ideaal maar het scheelt zo weinig dat we doen alsof. De fout die we dan maken is meestal gering.
Het doet er niet toe hoe groot de moleculen zijn. De natuurkundige Avogadro ontdekte aan het begin van de 19e eeuw (zeg maar 200 jaar geleden) het volgende:
Gelijke volumes van verschillende gassen bevatten evenveel moleculen.
Elk gas bij dezelfde temperatuur en druk.
Hij ontdekte ook hoeveel moleculen er in 1 mol zitten: 6,02 . 1023
We noemen dit aantal, het aantal deeltjes in 1 mol gas: de Avogadroconstante. Symbool: NA.
Bij standaard druk (1 atm; 1,013 bar; 1,013.105 Pa) en standaard temperatuur (0oC; 273,15 K) neemt een mol van een gas een volume in van 22,4 liter.
We noemen dit: het molair gasvolume.
